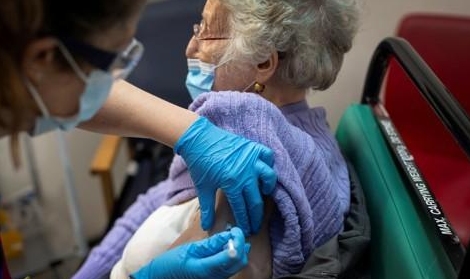
[사진=로이터·연합뉴스]
정부가 아스트라제네카의 신종 코로나바이러스 감염증(코로나19) 백신을 우리나라에 들여오는 것과 관련, 미국 식품의약품(FDA)의 승인 여부에 영향을 받지않을 것이란 입장을 밝혔다.
아스트라제네카 코로나19 백신에 대한 미국FDA의 승인이 지연되면서 내년 1분기로 계획된 국내 도입 일정도 무산되는 것이 아니냐는 일각의 우려를 일축한 것으로 보인다.
권준욱 중앙방역대책본부 2부본부장은 15일 온라인 정례 브리핑에서 아스트라제네카의 코로나19 백신 도입과 관련한 질문에 "미국 FDA 승인 여부와 상관없이 우리나라의 절차에 따라서 진행된다"고 말했다.
다만 권 2부본부장은 접종 시기와 관련한 질의에서는 "여러 협상 단계, 또 기술적인 측면 등을 고려하면 확보, 접종 시기는 가변적일 수 있다"고 답했다.
앞서 정부는 백신 공동구매·배분을 위한 국제 프로젝트인 '코백스 퍼실리티'(COVAX facility)를 통해 1000만명분, 글로벌 제약사와 개별 협상을 통해 3400만명분 등 총 4천400만명분의 백신을 확보하고 내년 1분기부터 순차 도입하겠다는 계획을 내놨다.
정부와 협상을 벌이고 있는 글로벌 제약사는 아스트라제네카, 화이자, 존슨앤존슨-얀센, 모더나 등 총 4개사다. 이중 국내 가장 빨리 도입되는 것은 아스트라제네카가 개발 중인 백신이다.
아스트라제네카는 지난 7월 국내 기업인 SK케미칼의 자회사 SK바이오사이언스와 코로나19 백신 생산을 위한 위탁생산 계약을 맺은 바 있다. 국내 생산공장을 두고 있어 유통·관리 측면에서 수월할 것으로 평가되고 있다.
하지만 아스트라제네카 백신은 최근 임상 발표 과정에서 투약 실수를 인정해 미국FDA로부터 효능과 안정성을 검증하기 위한 임상시험 과정이 투명하지 않았다는 불신을 초래했다.
최근 뉴욕타임즈, CNN 등 주요 외신은 미국FDA가 아스트라제네카 승인을 내년을로 미룰 수도 있다는 비관적인 관측을 내놨다.
반면 화이자-바이오엔테크는 FDA의 긴급사용 승인을 받아 지난 14일부터 미국 전역에서 백신 접종을 시작했다.
모더나도 이르면 오는 18일 FDA의 긴급사용 승인을 받을 것으로 전망되고 있다.








![[포토] 제8회 서민금융포럼](https://image.ajunews.com/content/image/2024/11/21/20241121114536531007_518_323.jpg)
![[포토] 기조연설 하는 페이커 이상혁](https://image.ajunews.com/content/image/2024/11/20/20241120115246771576_518_323.jpg)
![[포토] 발왕산은 벌써 겨울](https://image.ajunews.com/content/image/2024/11/19/20241119205226273772_518_323.jpg)
![[슬라이드 포토] 제44회 황금촬영상 시상식 참석한 스타들](https://image.ajunews.com/content/image/2024/11/18/20241118194949259743_518_323.jpg)


