
김대기 교수
미래창조과학부는 중소기업 메드팩토가 순수 국내 기술로 개발한 항암신약 후보물질로 종양성장인자 수용체 억제제인 TEW-7197이 최근 미국 FDA로부터 임상 1상 시험 승인을 받아 이달부터 미국 현지 임상시험에 착수했다고 19일 밝혔다.
이 물질은 미래부 신약후보물질 발굴 및 최적화사업 지원으로 김대기 이화여자대학교 교수팀이 도출한 후 메드팩토에 기술이전한 물질로 2013년 10월 보건복지부의 시스템통합적 항암신약개발사업단 과제로 선정돼 글로벌 항암제를 목표로 개발되고 있다.
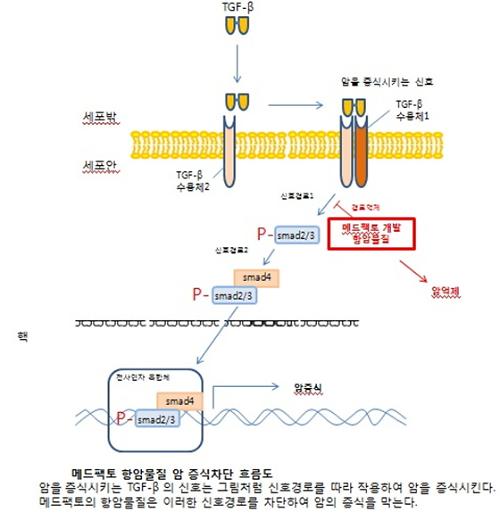
이 물질은 간암, 유방암 등 고형암 진행을 촉진시키는 수용체 ALK-5를 억제하는 화합물질로 암의 전이를 저해시키고 인체면역 기능을 활성화해 암세포를 죽이는 효과가 있는 것으로 알려졌다.
세계적으로 현재 미국의 제약사 한 곳에서 이 물질과 같은 표적으로 항암제 개발을 진행중으로 지금까지 비임상시험 결과로만 볼 때 미국 물질보다 효능과 안전성 측면에서 상대적으로 우월한 것으로 판단된다는 것이 연구팀의 설명이다.
이러한 우수 물질이 첫 글로벌 항암 신약으로 개발되면 향후 약 84조원 규모의 세계 항암제 시장에서 일정 지분을 확보할 수 있을 것으로 기대된다.
이번 연구 성과는 국내대학에서 개발한 신약 원천기술을 활용해 국내 기업이 미국 FDA 임상 1상 허가를 받았다는데 의미가 있는 것으로 국내 신약개발 수준의 발전을 상징한다.
이 연구는 미래부의 원천연구결과가 보건복지부의 임상시험 지원 사업으로 연계돼 부처 간 단절 없는 연계 지원의 대표적인 성공사례로 꼽힌다.
암은 1983년 이후 사망원인 1위를 차지하고 있는 가운데 이로 인한 직간접적 비용은 2005년 기준 14조원으로 경제·사회적 부담이 매년 증가하고 있다.
정부는 암부담을 줄이고 건강 보호를 위해 국산 항암제 개발 등 바이오・보건의료 기술개발 지원을 지속적으로 확대해나갈 예정이다.









![[포토] 눈 쌓인 덕수궁](https://image.ajunews.com/content/image/2024/11/27/20241127082949997862_518_323.jpg)
![[포토] 화성시 화재현장 합동감식](https://image.ajunews.com/content/image/2024/11/26/20241126123450357646_518_323.jpg)
![[포토] 법원, 이재명 위증교사 1심 무죄 선고](https://image.ajunews.com/content/image/2024/11/25/20241125145229136612_518_323.jpg)
![[포토] 법원 출석하는 이재명 대표](https://image.ajunews.com/content/image/2024/11/25/20241125140609985611_518_323.jpg)


