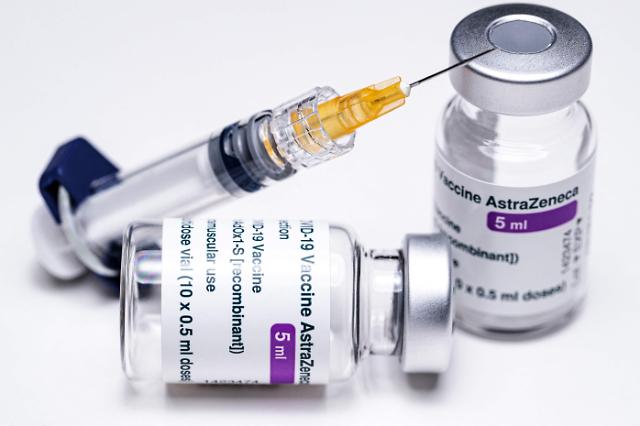
아스트라제네카(AZ) 신종 코로나바이러스 감염증(코로나19) 백신. [사진=AFP·연합뉴스]
글로벌 제약사 아스트라제네카(AZ)가 최근 발표한 신종 코로나바이러스 감염증(코로나19) 백신 임상시험 결과에 대한 새로운 자료를 48시간 이내에 제출하겠다고 23일(이하 현지시간) 밝혔다.
AZ 측의 이번 발표는 전날 미국 보건당국이 AZ 코로나19 백신 임상시험 결과에 오래된 정보가 포함됐을 수 있다고 우려한 뒤에 나왔다.
AZ 바이오의약품 사업부의 루드 도베어 사장은 전날 미국 경제전문매체 CNBC 방송에서 “4월 초에 (미국 내) 긴급사용 승인을 신청할 계획”이라면서 미국 당국의 결정에 따라 승인 시점이 결정될 것이라고 말했다.
도베어 사장은 미국 내 긴급승인이 신속하게 이뤄지면 3000만회 접종분을 인도하기를 희망한다고 했다.
영국 BBC방송은 AZ의 코로나19 백신 미국 임상시험 결과 발표가 미국 식품의약처(FDA) 긴급사용 승인에 결정적인 역할을 할 것이라며 4월 중순 AZ 백신 미국 사용 승인에 기대를 걸었다.
하지만 미국 보건당국이 AZ 임상시험 결과 발표 하루 만에 문제점을 제기했다. 국립알레르기전염병(NIAID) 연구소는 “AZ와 함께 실험을 수행하는 독립적인 모니터링 기관이 회사가 효능을 산출하는 데 쓴 데이터가 오래된 데이터라며 최신의 데이터를 사용해 효능을 산출할 것을 촉구했다”고 지적했다.
앤서니 파우치 NIAID 소장 역시 “(AZ의) 임상시험 결과를 평가하는 독립기관인 미국 데이터·안전모니터링위원회(DSMB)가 AZ의 언론 발표를 본 뒤 임상자료가 다소 시간이 지나 ‘약간’의 오해를 부를 수 있다고 우려했다”고 말했다.
그러면서 AZ 측이 보도자료의 내용이 맞는다는 것을 증명하고자 DSMB에 정확한 자료를 제출해야 한다고 덧붙였다.
AZ 측은 DSMB의 지적에 보도자료를 통해 발표한 결과는 지난 2월 17일까지의 시험 데이터를 중간 분석한 결과라고 밝히며, DSMB와 ‘가장 최신의 효능 데이터’를 논의하고 그 결과를 48시간 이내에 발표하겠다고 했다.
그러나 샌디에이고 스크립스리서치(Scripps Research)의 임상시험 전문가인 에릭 토플(Eric Topol)은 파이낸셜타임스(FT)에 AZ가 즉각 해당 문제를 해결해야 한다면서 “AZ는 48시간 내가 아닌 지금 당장 답을 내놔야 한다”고 목소리를 높였다.
한편 미국 보건당국의 이번 지적이 AZ 코로나19 백신의 미국 내 긴급사용 승인의 걸림돌이 될 것이란 우려가 등장했고, 이는 주가 하락으로 이어졌다. AZ 주가는 이날 뉴욕 나스닥 시장에서 전일 대비 1.80달러(3.52%) 빠진 49.40달러로 거래를 마쳤다.










![[포토] 경제부총리-외교장관 합동 외신기자 간담회](https://image.ajunews.com/content/image/2024/12/18/20241218113554802359_518_323.jpg)
![[포토] 아침 추위가 빚은 풍경](https://image.ajunews.com/content/image/2024/12/17/20241217114825954467_518_323.jpg)
![[포토] 한동훈, 당 대표직 사퇴합니다](https://image.ajunews.com/content/image/2024/12/16/20241216114507341351_518_323.jpg)
![[포토] 서울구치소 향하는 조국 전 대표](https://image.ajunews.com/content/image/2024/12/16/20241216115309417644_518_323.jpg)


