세계 첫 코로나19 백신 접종을 시작한 영국에서 전신 알러지 쇼크를 전력이 있을 경우 접종 대상에서 제외하기로 했다. 접종 첫날 2명이 부작용으로 알러지 반응을 보인 데 따른 것이다.

9일(현지시간) 로이터와 BBC 등 외신에 따르면, 이날 준 레인 영국 의약품건강관리제품규제청(MHRA) 청장은 "백신, 의약품, 식품에 대해서 아나필락시스 전력이 있는 사람은 화이자-바이오엔테크 백신을 접종해선 안 된다"고 발표했다.
아나필락시스란 급성 알레르기 반응의 일종으로, 특정 음식이나 약물 등 화학물질의 영향에 따른 인체의 과도한 항원-항체 면역 반응이다.
아나필락시스 쇼크가 일어날 경우, 전신에 두드러기나 혈관부종 등 피부 증상, 호흡 곤란, 혈압 감소, 의식소실 등과 같은 급성 증세를 보인다. 증상이 심각할 경우 생명을 위협할 수도 있다.
전날 화이자가 개발한 코로나19 백신인 BNT-163b2 접종을 시작한 영국에서 영국 국민보건서비스(NHS) 소속 직원 2명이 백신 접종 후 부작용으로 아나필락시스 증상을 보였다고 보고됐다. 이 외에도 일반 알레르기 반응으로 추정되는 부작용 사례도 1건이 보고됐다.
이에 따라 앞서 MHRA는 화이자 백신 접종 시작 이후 부작용 조사가 진행되는 동안 과거 약품이나 음식, 백신 등과 관련해 '중대한 알레르기 반응'(significant allergic reaction)을 보였던 이들은 접종을 하지 말아야 한다는 잠정 지침을 발표하기도 했다. 이후 MHRA은 하루도 채 지나지 않아 신속하게 해당 지침을 구체화한 것이다.
이와 관련해 레인 청장은 "여전히 화이자 백신의 안전성과 효과성에 대해서는 전적으로 신뢰할 수 있다"고 평가하면서 "1회차 접종 이후 아나필락시스를 경험할 경우 2회차 접종이 이뤄져서는 안 된다"고 강조했다.
그는 이어 "접종자 대부분은 아나필락시스 반응을 겪지 않을 것이며, 코로나19 감염 보호의 이점이 부작용 리스크보다 더 크다"며 "여전히 화이자의 백신이 MHRA의 안전, 품질, 효과성에 관한 견고한 기준을 충족했다는 점을 완전히 신뢰할 수 있다"고 설명했다.
다만, 같은 날 화이자 측이 과거 3상 임상시험에서 알레르기 이력이 있는 경우 시험 참여를 거부했던 것이 알려져 논란이 되기도 했다. 특히, 아나필락시스 유경험자는 시험 대상에서 완전히 배제된 사실도 전해져, 알레르기 전력자에 대한 백신 안전성이 검증되지 않았다는 우려를 키우기도 했다.
미국 식품의약국(FDA)이 지난 8일 공개한 자료에 따르면, 3상 임상 등록 참가자 4만4000여명 중 화이자의 백신 접종 후 과민성 부작용이 나타난 경우는 0.63%로 위약군(0.51%)보다 약간 높은 수준이었다.

준 레인 영국 의약품건강관리제품규제청(MHRA) 청장.[사진=영국 정부 홈페이지]
9일(현지시간) 로이터와 BBC 등 외신에 따르면, 이날 준 레인 영국 의약품건강관리제품규제청(MHRA) 청장은 "백신, 의약품, 식품에 대해서 아나필락시스 전력이 있는 사람은 화이자-바이오엔테크 백신을 접종해선 안 된다"고 발표했다.
아나필락시스란 급성 알레르기 반응의 일종으로, 특정 음식이나 약물 등 화학물질의 영향에 따른 인체의 과도한 항원-항체 면역 반응이다.
아나필락시스 쇼크가 일어날 경우, 전신에 두드러기나 혈관부종 등 피부 증상, 호흡 곤란, 혈압 감소, 의식소실 등과 같은 급성 증세를 보인다. 증상이 심각할 경우 생명을 위협할 수도 있다.
전날 화이자가 개발한 코로나19 백신인 BNT-163b2 접종을 시작한 영국에서 영국 국민보건서비스(NHS) 소속 직원 2명이 백신 접종 후 부작용으로 아나필락시스 증상을 보였다고 보고됐다. 이 외에도 일반 알레르기 반응으로 추정되는 부작용 사례도 1건이 보고됐다.
이에 따라 앞서 MHRA는 화이자 백신 접종 시작 이후 부작용 조사가 진행되는 동안 과거 약품이나 음식, 백신 등과 관련해 '중대한 알레르기 반응'(significant allergic reaction)을 보였던 이들은 접종을 하지 말아야 한다는 잠정 지침을 발표하기도 했다. 이후 MHRA은 하루도 채 지나지 않아 신속하게 해당 지침을 구체화한 것이다.
이와 관련해 레인 청장은 "여전히 화이자 백신의 안전성과 효과성에 대해서는 전적으로 신뢰할 수 있다"고 평가하면서 "1회차 접종 이후 아나필락시스를 경험할 경우 2회차 접종이 이뤄져서는 안 된다"고 강조했다.
그는 이어 "접종자 대부분은 아나필락시스 반응을 겪지 않을 것이며, 코로나19 감염 보호의 이점이 부작용 리스크보다 더 크다"며 "여전히 화이자의 백신이 MHRA의 안전, 품질, 효과성에 관한 견고한 기준을 충족했다는 점을 완전히 신뢰할 수 있다"고 설명했다.
다만, 같은 날 화이자 측이 과거 3상 임상시험에서 알레르기 이력이 있는 경우 시험 참여를 거부했던 것이 알려져 논란이 되기도 했다. 특히, 아나필락시스 유경험자는 시험 대상에서 완전히 배제된 사실도 전해져, 알레르기 전력자에 대한 백신 안전성이 검증되지 않았다는 우려를 키우기도 했다.
미국 식품의약국(FDA)이 지난 8일 공개한 자료에 따르면, 3상 임상 등록 참가자 4만4000여명 중 화이자의 백신 접종 후 과민성 부작용이 나타난 경우는 0.63%로 위약군(0.51%)보다 약간 높은 수준이었다.

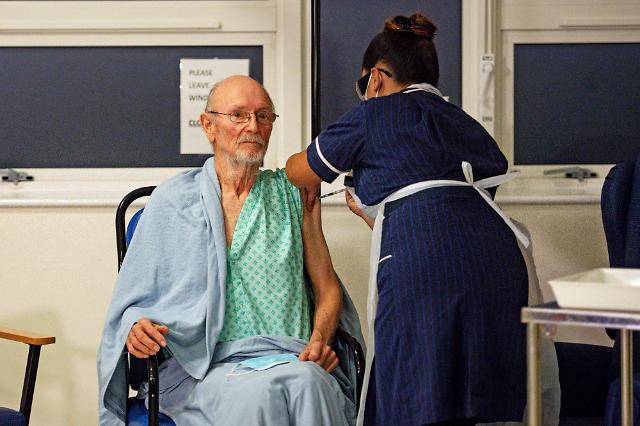
지난 8일(현지시간) 영국에서 세계 첫 코로나19 백신 접종을 시작한 가운데, 세계에서 2번째로 화이자바이오엔테크가 개발한 백신을 접종한 81세 윌리엄 셰익스피어.[사진=로이터·연합뉴스]




![[K-배터리 도전 직면] 완성차 잇단 마이웨이... LG·SK·삼성 파운드리 공장 되나](https://image.ajunews.com/content/image/2025/03/14/20250314061807664275_388_136.png)




![[슬라이드 포토] 故 휘성, 영정 사진 속 환한 미소](https://image.ajunews.com/content/image/2025/03/14/20250314131052257994_518_323.jpg)
![[포토] 홈플러스, 정산 대금 3400억 지급…현금 1600억 보유](https://image.ajunews.com/content/image/2025/03/14/20250314104411947330_518_323.jpg)
![[포토] 최재해 감사원장, 기각 후 업무 복귀](https://image.ajunews.com/content/image/2025/03/13/20250313120924594304_518_323.jpg)
![[포토] 국민의힘, 헌재 앞 기자회견](https://image.ajunews.com/content/image/2025/03/13/20250313120803802996_518_323.jpg)


