
서울의 한 쇼핑몰 내 음식점에 일반음식점 핵심방역 수칙 관련 안내문이 붙어 있다.[사진=연합뉴스]
식품의약품안전처는 신종 코로나바이러스 감염증(코로나19) 감염 여부를 30분 만에 알 수 있는 에스디바이오센서의 진단키트(진단시약) 2종을 정식 허가했다고 11일 밝혔다.
코로나19 진단엔 분자진단(RT-PCR)과 면역진단인 항체진단, 항원진단 방식이 있다. RT-PCR 검사 방식 이외에 항원·항체 진단 방식 제품이 국내에서 허가된 건 이번이 처음이다.
이번에 허가한 진단키트는 의료인이나 검사전문가가 사용하는 제품이다. 항체 진단키트는 검사자의 혈액 속에 들어있는 여러 항체들을 분리한 후 이 중 코로나19 바이러스 감염 시 만들어지는 항체도 들어있는지 확인하는 방식이다. 검사시간은 15분 내외다. 과거 감염 이력도 확인할 수 있어 해외 출입국 시 제출용, 면역 획득 여부 확인용으로 쓰일 것으로 보인다. 다만 코로나19 바이러스가 지금 존재하는지는 알 수 없다는 한계가 있다.
이번 허가 조치로 국내 시판 가능한 진단키트는 RT-PCR 진단키트 5개, 항원 진단키트 1개, 항체 진단키트 1개 등 총 5개 업체 7개 제품이 됐다.
전날 기준 정식허가를 신청한 진단키트는 RT-PCR 방식 14개, 항원진단 4개, 항체진단 11개로 총 29개 제품이 심사 단계에 있다.
식약처 관계자는 “국내외 코로나19 진단키트의 개발 동향을 지속적으로 모니터링하고 있다”며 “품질이 우수한 제품을 신속하게 허가해 국민이 진단과 치료 기회를 보장받을 수 있도록 하겠다”고 말했다.
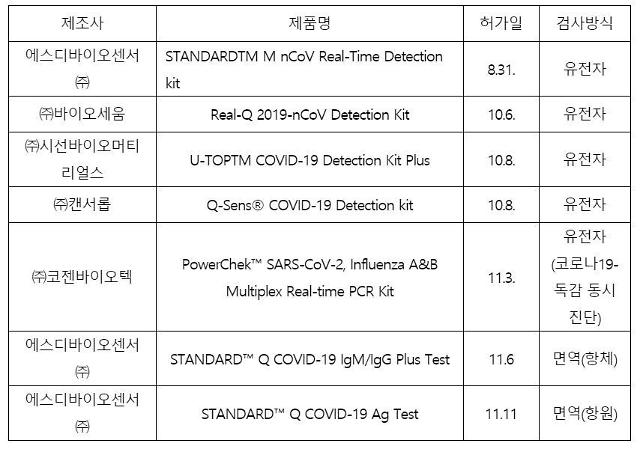
지난 10일 기준 코로나19 진단키트 허가 제품 7종 목록.[자료=식품의약품안전처 제공]








![[날씨] 전국 흐리고 눈비…미세먼지는 좋음](https://image.ajunews.com/content/image/2025/03/16/20250316062142985743_388_136.jpg)
![[슬라이드 포토] 故 휘성, 영정 사진 속 환한 미소](https://image.ajunews.com/content/image/2025/03/14/20250314131052257994_518_323.jpg)
![[포토] 홈플러스, 정산 대금 3400억 지급…현금 1600억 보유](https://image.ajunews.com/content/image/2025/03/14/20250314104411947330_518_323.jpg)
![[포토] 최재해 감사원장, 기각 후 업무 복귀](https://image.ajunews.com/content/image/2025/03/13/20250313120924594304_518_323.jpg)
![[포토] 국민의힘, 헌재 앞 기자회견](https://image.ajunews.com/content/image/2025/03/13/20250313120803802996_518_323.jpg)


