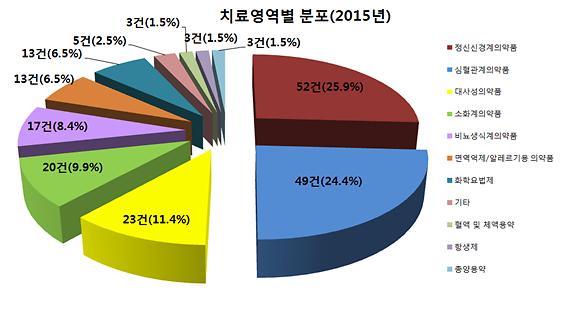
[식품의약품안전처 제공]
식품의약품안전처는 2015년 제네릭의약품 개발동향을 분석한 결과 전체 생물학적동등성(이하 ‘생동성’) 시험계획 승인 201건 가운데, 정신신경계의약품과 심혈관계의약품이 각각 52건(25.9%), 49건(24.5%)로 1~2위를 차지했다고 23일 밝혔다.
생동성 시험이란 생물학적 동등성을 입증하기 위한 생체실험으로 동일 주성분을 함유한 두 제제의 생체이용률이 통계학적으로 동등하다는 것을 보여주는 시험이다.
대사성의약품 승인도 23건으로 전체의 11.4%를 차지했다. 이어 소화계의약품 20건(9.9%), 비뇨‧생식기계의약품 17건(8.4%), 화학요법제 13건(6.5%) 등으로 높았다.
비뇨‧생식기계의약품의 경우 지난 2014년에는 타다라필 등의 특허만료로 33건이었지만 지난해에는 17건으로 개발이 주춤했다.
지난해 재심사 또는 특허만료 예정인 제네릭의약품 개발을 위한 생동성시험 승인건수는 148건으로 전체(201건)의 73.6%에 달했다.
올해 6월 재심사가 만료되는 고혈압치료제 '텔미사르탄'과 , '암로디핀 복합제'가 11건으로 가장 많았고 뇌기질성 정신증후군에 사용되는 '콜린알포세레이트'와 치매치료제 '도네페질'이 각각 그 뒤를 이었다.
자세한 생동성 승인 현황은 '온라인의약도서관'에서 확인할 수 있다.







![[날씨] 최고 12도 포근…경상·제주 눈·비 소식](https://image.ajunews.com/content/image/2025/02/01/20250201170825722142_388_136.jpg)
![[포토] 문재인 전 대통령 예방한 이재명 대표](https://image.ajunews.com/content/image/2025/01/30/20250130223539232209_518_323.jpg)
![[포토] 美구조당국, 워싱턴 여객기·헬기 추락사고 생존자 없는 듯](https://image.ajunews.com/content/image/2025/01/30/20250130223233798113_518_323.jpg)
![[포토] 검게 탄 화재 여객기](https://image.ajunews.com/content/image/2025/01/29/20250129121436828718_518_323.jpg)
![[포토] 김해공항서 에어부산 항공기 꼬리에 불…인명피해 없어](https://image.ajunews.com/content/image/2025/01/28/20250128230321338536_518_323.jpg)


